Ácidos e Bases: Aplicações e Segurança: 5 Exemplos De Ácidos E Bases Com Suas Respectivas Utilizacoes

Exemplos De Ácidos E Bases Com Suas Respectivas Utilizacoes – Ácidos e bases são substâncias químicas fundamentais presentes em diversos aspectos da nossa vida, desde a indústria até os processos biológicos do nosso corpo. Compreender suas propriedades e aplicações é crucial para o desenvolvimento tecnológico e para a segurança no manuseio destes compostos. Esta discussão explorará os conceitos básicos de ácidos e bases, apresentará exemplos de ácidos e bases fortes e fracas, suas aplicações, as reações ácido-base, e, crucialmente, as medidas de segurança necessárias para o seu manuseio.
Conceitos Básicos de Ácidos e Bases
A definição de ácido e base evoluiu ao longo do tempo. Segundo Arrhenius, um ácido é uma substância que, em solução aquosa, libera íons hidrogênio (H+), enquanto uma base libera íons hidroxila (OH-). A teoria de Brønsted-Lowry amplia essa definição, considerando ácido como um doador de prótons (H+) e base como um receptor de prótons. A importância do pH reside na sua capacidade de quantificar a concentração de íons H+ em uma solução, classificando-a como ácida (pH < 7), neutra (pH = 7), ou básica (pH > 7). A escala de pH varia de 0 a 14, sendo 0 extremamente ácido e 14 extremamente básico.
Exemplos de Ácidos e suas Aplicações, 5 Exemplos De Ácidos E Bases Com Suas Respectivas Utilizacoes
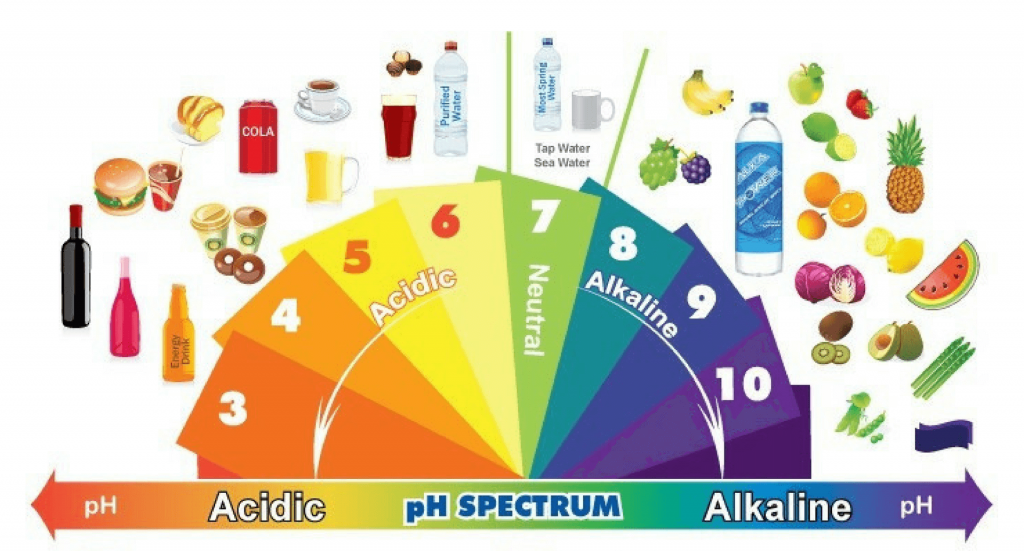
Ácidos fortes e fracos se diferenciam pela sua capacidade de ionização em água. Ácidos fortes se ionizam completamente, enquanto ácidos fracos se ionizam parcialmente. Esta diferença afeta significativamente suas propriedades e aplicações.
| Nome do Ácido | Fórmula Química | Propriedades | Aplicações |
|---|---|---|---|
| Ácido Clorídrico | HCl | Forte, corrosivo, altamente reativo. | Produção de cloreto de vinila (PVC), limpeza industrial, produção de outros compostos químicos. |
| Ácido Sulfúrico | H₂SO₄ | Forte, corrosivo, desidratante. | Produção de fertilizantes, baterias de chumbo-ácido, refinação de petróleo. |
Abaixo, exemplos de ácidos fracos:
- Ácido Acético: CH₃COOH
- Propriedades: Fraco, corrosivo em altas concentrações, odor característico de vinagre.
- Aplicações: Produção de vinagre, conservante de alimentos, indústria têxtil.
- Ácido Cítrico: C₆H₈O₇
- Propriedades: Fraco, sabor azedo, encontrado naturalmente em frutas cítricas.
- Aplicações: Aditivo alimentar, conservante, agente quelante.
Comparando um ácido forte (como o ácido clorídrico) e um ácido fraco (como o ácido acético), notamos que o ácido forte possui maior capacidade de ionização, resultando em maior concentração de íons H+ em solução e, consequentemente, maior acidez e maior poder corrosivo. As aplicações refletem essas diferenças: ácidos fortes são usados em processos industriais que exigem alta reatividade, enquanto ácidos fracos encontram aplicações em áreas onde a reatividade mais suave é necessária, como na indústria alimentícia.
Exemplos de Bases e suas Aplicações
Similarmente aos ácidos, as bases fortes se ionizam completamente em água, enquanto as bases fracas o fazem parcialmente. Esta diferença impacta suas propriedades e aplicações.
| Nome da Base | Fórmula Química | Propriedades | Aplicações |
|---|---|---|---|
| Hidróxido de Sódio | NaOH | Forte, corrosivo, altamente solúvel em água. | Produção de sabão, papel, têxteis, limpeza industrial. |
| Hidróxido de Cálcio | Ca(OH)₂ | Forte, menos solúvel em água que o NaOH. | Construção civil (cal hidratada), tratamento de água, agricultura. |
A seguir, exemplos de bases fracas:
- Amônia: NH₃
- Propriedades: Fraca, odor pungente, gasosa à temperatura ambiente.
- Aplicações: Fertilizantes, produção de plásticos, limpeza doméstica.
- Hidróxido de Magnésio: Mg(OH)₂
- Propriedades: Fraca, pouco solúvel em água, usado como antiácido.
- Aplicações: Medicamentos para azia e queimação estomacal, laxante.
Comparando uma base forte (como o hidróxido de sódio) e uma base fraca (como a amônia), observamos que a base forte possui maior capacidade de liberar íons OH- em solução, resultando em maior basicidade e maior poder corrosivo. As aplicações refletem essa diferença, com bases fortes utilizadas em processos industriais robustos e bases fracas em aplicações onde a reatividade mais suave é desejada, como em medicamentos.
Reações Ácido-Base e suas Aplicações

A reação de neutralização ocorre quando um ácido reage com uma base, produzindo sal e água. Um exemplo clássico é a reação entre o ácido clorídrico (HCl) e o hidróxido de sódio (NaOH):
HCl(aq) + NaOH(aq) → NaCl(aq) + H₂O(l)
A titulação ácido-base é um método analítico quantitativo usado para determinar a concentração de uma solução ácida ou básica, utilizando uma solução de concentração conhecida (solução padrão). É um processo fundamental em química analítica.
Para determinar a concentração de um ácido desconhecido usando uma base de concentração conhecida (titulação), seguem-se os passos:
- Preparar a solução de base de concentração conhecida.
- Medir um volume preciso da solução ácida desconhecida.
- Adicionar algumas gotas de indicador ácido-base (fenolftaleína ou outro indicador apropriado).
- Titular a solução ácida com a solução básica, adicionando gota a gota até a mudança de cor do indicador.
- Registrar o volume da base gasto para atingir o ponto de equivalência.
- Calcular a concentração do ácido desconhecido usando a estequiometria da reação e os volumes gastos.
Segurança no Manuseio de Ácidos e Bases
Ácidos e bases fortes podem causar sérios danos à pele, olhos e mucosas. O manuseio inadequado pode resultar em queimaduras químicas graves, irritações e até cegueira. É fundamental seguir rigorosamente as normas de segurança.
Normas de segurança para o trabalho com ácidos e bases em laboratório incluem:
- Uso obrigatório de equipamentos de proteção individual (EPI), como luvas resistentes a químicos, óculos de proteção, avental e máscara.
- Realizar os experimentos em capela de exaustão para evitar a inalação de vapores.
- Manter os recipientes devidamente identificados e armazenados em locais apropriados.
- Nunca adicionar água a ácidos concentrados; sempre adicionar o ácido à água lentamente e sob agitação.
- Em caso de derramamento, seguir os procedimentos de emergência específicos para cada substância.
Em caso de contato com ácidos ou bases fortes na pele ou olhos, lave imediatamente a área afetada com grande quantidade de água corrente por pelo menos 15 minutos e procure atendimento médico imediatamente. A rapidez na lavagem é crucial para minimizar os danos.
De refrigerantes a medicamentos, de limpeza doméstica à produção industrial, a presença de ácidos e bases é inegável e essencial. Compreender suas propriedades e aplicações é fundamental, não apenas para a ciência, mas também para a segurança e o desenvolvimento tecnológico. A exploração destes cinco exemplos, embora representando apenas uma pequena fração da vasta gama de ácidos e bases existentes, ilumina a importância do equilíbrio químico e a necessidade de um manuseio cuidadoso dessas substâncias poderosas.
A próxima vez que você usar um produto de limpeza ou saborear um alimento ácido, lembre-se da complexa química que torna tudo isso possível. E, lembre-se sempre: segurança em primeiro lugar.

